AstraZeneca, riunione Aifa-ministero per nuove indicazioni sull'utilizzo
di Alessandro Bacci
Per una decisione definitiva, però, bisognerà attendere il pronunciamento dell'Agenzia europea dei medicinali Ema, atteso entro giovedì
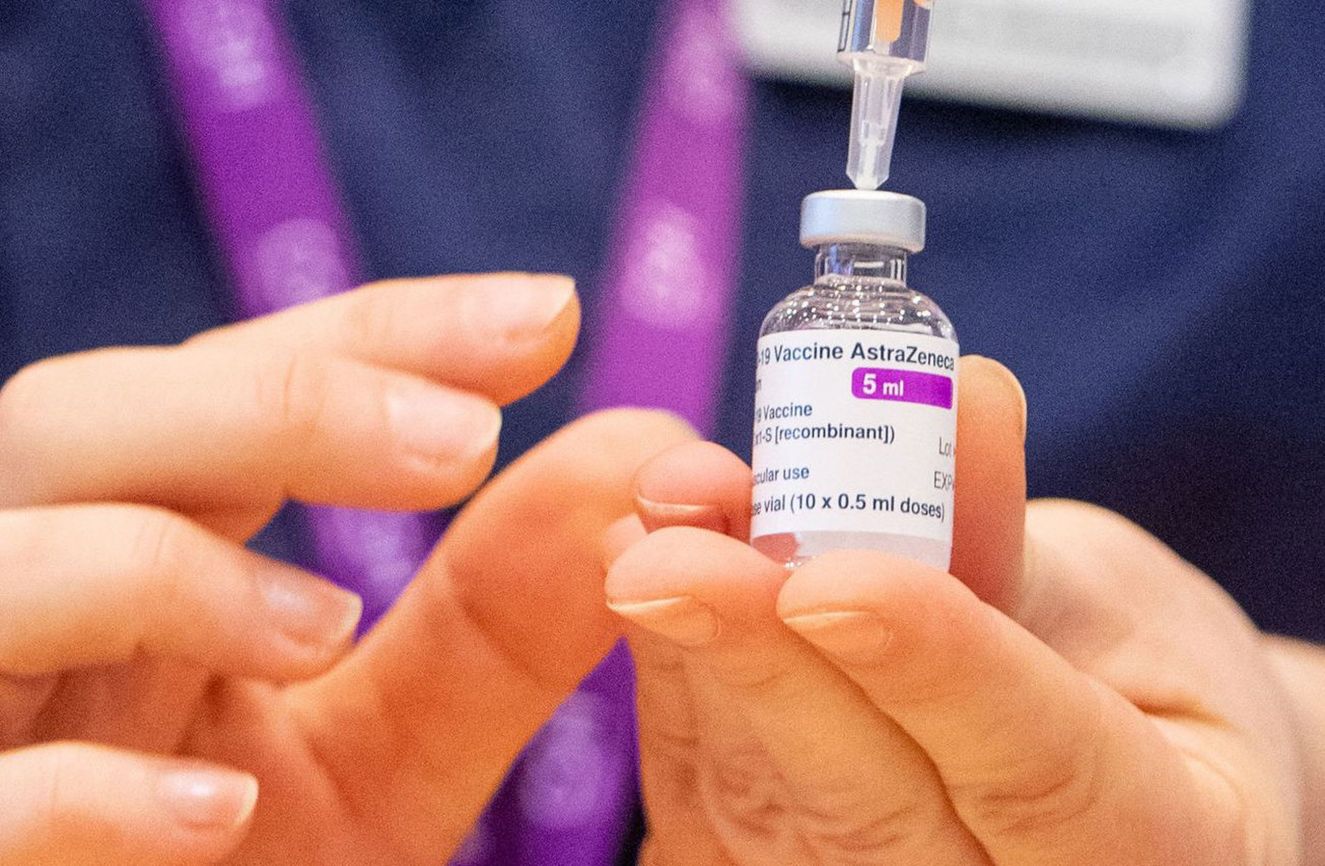
Si terrà oggi nel tardo pomeriggio, secondo quanto confermano alcune fonti, una riunione tra i tecnici dell'Agenzia italiana del farmaco (Aifa) e ministero della Salute in merito ad eventuali ulteriori indicazioni sull'utilizzo del vaccino anti-Covid di AstraZeneca.
Per una decisione, tuttavia, si attenderà il pronunciamento dell'Agenzia europea dei medicinali Ema, atteso entro giovedì, sull'eventuale correlazione tra il vaccino ed i rarissimi eventi trombotici segnalati in vari Paesi. In Italia hanno fatto discutere due morti di trombosi avvenute in due giorni consecutivi: uno a Genova, dove ha perso la vita una donna di 32 anni, e uno a Palermo, con il decesso di un 45enne. Entrambi avevano ricevuto la dose di AstraZeneca nelle scorse settimane ma per il momento non sembra esserci una correlazione tra morte e vaccino.
"È possibile, per maggiore precauzione, che l'Agenzia europea dei medicinali Ema indichi che per una determinata categoria è meglio non utilizzare il vaccino anti-Covid di AstraZeneca". Lo ha affermato a Radio 24 il sottosegretario alla Salute Pierpaolo Sileri, precisando tuttavia che "questo è successo anche per tanti altri famaci" e che nel caso di AstraZeneca il vaccino è stato utilizzato "in un numero estremamente alto di soggetti, mentre gli eventi trombotici rari segnalati sono pochissimi". "Non vi è ombra di dubbio che vi sia un rapporto rischio-beneficio positivo", ha aggiunto.
L'Ema, ha spiegato Sileri, "può cioè individuare dei sottogruppi di popolazione che presentano un come un denominatore per un maggiore livello di rischio, e valutare il rapporto causa-effetto in tali gruppi" in relazione agli eventi trombotici rari che sono stati segnalati. Quanto alla possibilità che l'Ema arrivi quindi a limitare l'uso del vaccino escludendo alcune categorie, ciò, ha sottolineato Sileri, "rientra nei processi di farmacovigilanza ed è già successo per tanti altri farmaci, a partire dall'aspirina, per la quale a partire dagli anni '80 è stato posto un limite d'uso per la fascia dei bambini sotto i 12 anni per alcuni eventi avversi".
Condividi:















